Статическое электричество
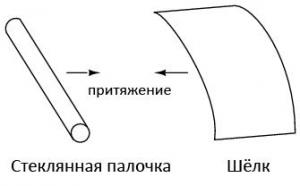
Не только шелк и стекло ведут себя подобным образом. Если потереть воздушный шарик, можно наблюдать, что латекс прилипает к рукам. Твердый парафин, и кусочек шерстяной ткани — еще одна пара материалов, между которыми была обнаружена сила притяжения.
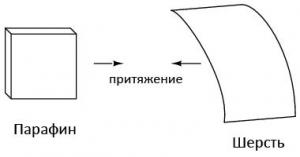
Подобное явление вызвало еще больший интерес, после того, как было обнаружено, что одинаковые материалы после трения одной и той же тканью всегда отталкиваются друг от друга.
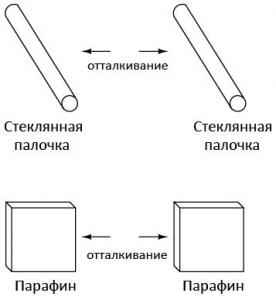
Было также замечено, что если кусочек стекла потереть шелковой тканью и приблизить его к кусочку воска, который потерли шерстью, эти предметы будут притягиваться друг к другу.
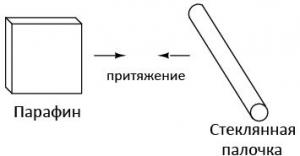
В дальнейшем ученые обнаружили, что любой материал, обладающий подобными свойствами притяжения и отталкивания, может быть причислен к одной из двух различных категорий: объекты, притягивающиеся к стеклу и отталкиваемые парафином или отталкиваемые стеклом и притягивающиеся к парафину. Как оказалось, третьего не дано: веществ, которые бы одновременно притягивались к парафину/стеклу или отталкивались от них, или реагировали только на один материал, не нашлось.
Пристальное внимание исследователей обратилось к кусочкам ткани, используемым для трения. Оказалось, что если потереть два кусочка стекла двумя кусочками шелка, отталкиваться друг от друга будут не только кусочки стекла, но и кусочки шелка. Подобное явление имело место и в случае с шерстью и воском.
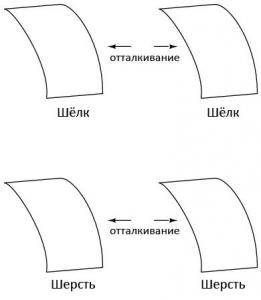
Что было действительно странно наблюдать. В конце концов, несмотря на то, что в результате трения ни один из этих объектов не подвергся видимым изменениям, изменились их свойства. Что именно заставило объекты отталкиваться или притягиваться, оставалось неизвестным.
Некоторые экспериментаторы высказывали догадки о том, что в результате трения объекты передают друг другу некие «флюиды», способные распространять физическую силу на расстоянии. Одним из первых экспериментаторов, наглядно показавших, что существует два типа изменения свойств материалов в результате трения друг о друга, был Шарль Дюфе. Тот факт, что в материалах происходит более одного вида изменений, стал очевидным благодаря возникающим в результате трения двум видам силы. Гипотетический обмен флюидами получил название заряда.
Один из пионеров подобных исследований, Бенджамин Франклин, пришел к выводу о том, что в результате трения между объектами возникает только один «флюид», а два различных «заряда» представляют собой лишь либо его избыток, либо недостаток. Проводя эксперименты с парафином и шерстью, Франклин предположил, что необработанная шерсть удаляет часть этого невидимого флюида с мягкого парафина, вызывая его избыток на кусочке шерсти и его недостаток на кусочке воска. Возникающее несоответствие в содержании флюида вызывает притяжение между шерстью и воском, поскольку флюид «пытается» восстановить исходное равновесие между двумя веществами.
Гипотеза о существовании одного «флюида», приобретаемого или утрачиваемого в результате трения, наилучшим образом подходила к наблюдаемым явлениям: все материалы точным образом подпадают под одну из категорий и, что самое главное, два активных материала, потертые друг о друга, всегда оказываются в противоположных категориях, что доказывается их неизменным притяжением друг к другу. Проще говоря, из всех проведенных экспериментов не было такого случая, чтобы потертые друг о друга материалы стали оба положительными или оба отрицательными.
В след за предположением Франклина о том, что шерсть «стирает» что-то с поверхности воска, тип «заряда», свойственный потертому воску был назван «отрицательным» (т.к. предположительно представлял собой недостаток флюида), тогда как тип заряда, свойственный кусочку шерсти получил название «положительного» (т.к. предположительно представлял собой избыток флюида). Он и не мог предположить, что его невинная догадка повлечет за собой такое смятение в рядах изучающих электричество.
Точно измерить электрический заряд удалось французскому физику Шарлю Кулону в 1780-х годах. Он использовал для этого особое устройство — крутильные весы — устройство для измерения силы, возникающей между двумя носителями электрического заряда (двумя заряженными предметами). Результатом исследования Кулона стало появление единицы электрического заряда, названной в его честь. Если два «целевых» объекта (гипотетические объекты не имеют значительной площади поверхности) с одинаковым зарядом 1 Кл поместить на расстоянии одного метра, они будут взаимодействовать с силой, равной около 9 миллиардов ньютонов, притягиваясь или отталкиваясь друг от друга в зависимости от типов зарядов. Определение кулона как единицы электрического заряда (в выражении силы взаимодействия точечных зарядов) оказалось равным избытку или недостатку примерно 6250000000000000000 электронов. Или, иначе говоря, один электрон имеет заряд около 0, 00000000000000000016 кулона. Принимая во внимание то, что электрон является наименьшим известным носителем электрического заряда, последняя цифра заряда электрона определяется как элементарный электрический заряд.
Намного позднее было открыто, что этот «флюид» на самом деле состоит из невероятно малых частиц, названных впоследствии электронами, что происходит от древнегреческого слова, означающего «янтарь», — ещё одно вещество, проявляющее зарядные свойства в результате трения. Дальнейшие эксперименты показали, что все объекты состоят из невероятно малых «строительных блоков» —атомов, которые в свою очередь состоят из еще меньших элементов —частиц. Три элементарные частицы, входящие в состав большинства атомов называются протоны, нейтроны и электроны. В большинстве атомов присутствует «набор» протонов, нейтронов и электронов, но существуют такие, в которых нейтроны отсутствуют. Примером может служить протий (1Н1)— изотоп водорода (Водород-1) — самая легкая и самая распространенная форма водорода, имеющая один протон и один электрон. Атомы слишком малы, чтобы их разглядеть, но если бы мы могли это сделать, мы бы увидели следующее:
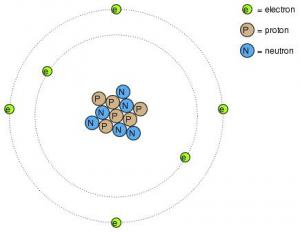
Несмотря на то, что каждый атом вещества представляет собой единое целое, на самом деле между электронами и скоплением протонов и нейтронов в середине имеется большое пустое пространство.
На рисунке в общем виде показан атом углерода, у которого шесть протонов, шесть нейтронов и шесть электронов. В каждом атоме протоны и нейтроны прочно соединены между собой, что очень важно. Скопление тесно прижатых друг к другу протонов и нейтронов в центре атома называется ядром, а число протонов в ядре атома определяет принадлежность атома к какому-либо из элементов. Изменение числа протонов в ядре атома повлечет за собой изменение типа атома. К примеру, если бы удалось изъять три протона из атома свинца, можно было бы осуществить древнюю мечту алхимиков — превратить его в атом золота! Тесное соединение протонов в ядре отвечает за стабильность состава химических элементов и означает крах мечты алхимиков.
Нейтроны в намного меньшей степени, чем протоны влияют на химические свойства и целостность атома, хотя их так же трудно удалить или добавить к ядру, поскольку они тесно прижаты. Если из атома убрать нейтроны или добавить их к нему, то его масса слегка изменится и он также может приобрести особые ядерные свойства, такие как радиоактивность.
Однако электроны обладают значительно большей свободой перемещения по поверхности атома, чем протоны или нейтроны. На самом деле их можно выбить из их мест (даже заставить их полностью покинуть атом!) при усилиях, гораздо меньших, чем те, что требуются для изменения местоположения частиц в ядре. При этом атом, сохраняя свою химическую целостность, становится значительно менее устойчивым. Электроны и протоны уникальны в своем свойстве притягивать друг друга на расстоянии. Именно их притяжение на расстоянии вызывает притяжение между объектами в результате трения — электроны отсоединяются от своих атомов и прикрепляются к атомам другого объекта.
Электроны отталкивают другие электроны на расстоянии, так же, как протоны ведут себя с другими протонами. Единственная причина, по которой протоны прижаты друг к другу в ядре атома — более мощная сила, которая проявляется только на малых расстояниях. Из-за такого притяжения/отталкивания между отдельными частицами считается, что электроны и протоны имеют противоположные электрические заряды. Таким образом, каждый электрон имеет отрицательный заряд, а каждый протон — положительный. Поскольку число протонов и электронов в атоме одинаково, они нейтрализуют друг друга, таким образом, суммарный заряд атома равен нулю. Поэтому на рисунке у атома углерода изображено шесть электронов: они уравновешивают электрический заряд шести протонов в ядре. При уменьшении или увеличении числа электронов суммарный заряд атома перестает быть нейтральным, атом становится «заряженным» в целом, вследствие чего начинает взаимодействовать с заряженными частицами и другими заряженными атомами рядом. Нейтроны не притягиваются и не отталкиваются электронами, протонами или даже другими нейтронами, вследствие чего расцениваются как незаряженные частицы.
Именно такой процесс потери и приобретения электронов происходит при трении отдельных веществ друг о друга. В результате трения электроны из атомов одного вещества переходят на атомы другого вещества. Иначе говоря, электроны и составляют те самые «флюиды», о которых говорил Бенджамин Франклин.
Результат дисбаланса этих «флюидов» (электронов) между объектами получил название «статическое электричество». Статическое потому, что электроны стремятся к неподвижности после перемещения с одного материала на другой. Как показали дальнейшие эксперименты с парафином и шерстью, на самом деле именно электроны шерсти уходят к атомам парафина, а не наоборот, как предполагал Франклин. Вслед за Франклином, говорившим об «отрицательном» заряде парафина и «положительном» заряде шерсти, сочли, что электроны несут «отрицательный» заряд. Таким образом, объект, атомы которого получают дополнительные электроны, именуется отрицательнозаряженным, тогда как объект, чьи электроны покинули свои места, именуется положительно заряженным, какими бы запутанными не казались эти определения. К тому времени, когда истинная природа электрических «флюидов» была открыта, терминология Франклина относительно электрического заряда слишком прочно закрепила свои позиции в научном мире, и поэтому применяется и по сей день.
Майкл Фарадей доказал (в 1832 г.), что статическое электричество имеет такую же природу, как и электричество, производимое батареей или генератором. Но в большинстве случаев статическое электричество является помехой. Для предупреждения воспламенения из-за статического электричества в черный порох и бездымный порох добавляют графит. Статическое электричество вызывает повреждения в чувствительных полупроводниковых схемах. Среди немногих примеров практического применения статического электричества можно назвать ксерокопирование, электростатический воздушный фильтр, и генератор высокого напряжения Ван де Граафа.
- РЕЗЮМЕ
- Все объекты состоят из мельчайших «строительных блоков», атомов.
- Все встречающиеся в природе атомы содержат частицы, называемыеэлектроны, протоны и нейтроны, за исключением протия — изотопа водорода (1Н1).
- Электроны являются носителями отрицательного (-) электрического заряда.
- Протоны являются носителями положительного (+) электрического заряда.
- Нейтроны не имеют электрического заряда.
- Электроны гораздо проще вытеснить из атомов, чем протоны или нейтроны.
- Число протонов в атомном ядре определяет его принадлежность к тому или иному химическому элементу.